A Epilepsia afeta aproximadamente 0,5 a 1% da população mundial. As crises e as síndromes epilépticas têm etiologias diversas. Em boa parte dos casos, não se consegue estabelecer uma causa definitiva.
No diagnóstico das síndromes epilépticas, a história clínica é um elemento fundamental, incluindo a caracterização das crises, o período pós-ictal, desencadeantes e gatilhos, o uso de substâncias, condições médicas prévias e a história familiar. O exame clínico e o neurológico são também essenciais.
Os exames complementares utilizados para a definição das síndromes epilépticas e suas etiologias incluem o eletroencefalograma, em todas as suas modalidades, exames laboratoriais, buscando anormalidades metabólicas ou infecciosas, e os exames de neuroimagem.
A ressonância magnética (RM) do encéfalo é o exame de imagem mais útil, podendo revelar lesões de natureza infecciosa, vascular e tumoral, além de processos específicos, como a Esclerose Mesial Temporal.
O exame do líquido cefalorraquidiano é útil nos seguintes contextos relacionados à definição etiológica das epilepsias:
Veja também: Reação em cadeia da polimerase (PCR) no diagnóstico das neuroinfecções.
1) Avaliação de primeira crise
A punção lombar (PL) e o exame do líquido cefalorraquidiano devem ser realizados em todos os pacientes em que há suspeita da crise ser secundária a um processo infeccioso.
A interpretação do exame deve ser feita de maneira cautelosa, visto que a crise em si pode causar pleocitose. Deve-se realizar exame de neuroimagem prévio, com o objetivo de excluir lesões expansivas que potencialmente contraindicam a PL.
Quando o líquido cefalorraquidiano mostra anormalidades inflamatórias, devem ser realizados exames específicos, seja para confirmação de etiologia infecciosa, seja autoimune. Em crianças com crises febris, o exame é necessário para exclusão de eventual Meningite ou Encefalite.
2) Crises epilépticas e infecções
Crises epilépticas podem ser sintoma de inúmeras infecções, incluindo infecções bacterianas (meningites agudas, abscesso cerebral, empiema epi ou subdural), Neurotuberculose (Meningite ou granulomas), infecções parasitárias (Neurocisticercose, Malária Cerebral, Neurotoxoplasmose), fungos (Meningites ou abscessos fúngicos) e vírus (Encefalites).
Além dos exames citobioquímico e microbiológico convencionais, vários exames no líquido cefalorraquidiano auxiliam nesses diagnósticos, como a detecção de anticorpos para T. solium e Toxoplasma, e a biologia molecular (PCR) para M. tuberculosis, fungos, vírus e bactérias.
A PCR pode ser realizada individualmente ou em painéis, com pesquisa simultânea de vários agentes infecciosos.
3) Epilepsia autoimune:
A Epilepsia Autoimune foi reconhecida pela “International League Against Epilepsy (ILAE)” como uma entidade distinta em 2017. Sua identificação é essencial para a instituição da imunoterapia.
A prevalência da Epilepsia Autoimune é de 13,7/100.000 indivíduos. As Epilepsias Autoimunes são desencadeadas por anticorpos anti-neuronais. Nos casos paraneoplásicos, pode haver uma neoplasia oculta.
Diferentes mecanismos, como mimetismo molecular (com ou sem infecção prévia conhecida) e disseminação do epítopo, são postulados como desencadeadores.
A apresentação clínica é de uma Epilepsia tardia e refratária, podendo ou não haver outros sintomas encefálicos, como manifestações neuropsiquiátricas, cognitivas e pródromos virais.
O escore APE2 (“Antibody Prevalence in Epilepsy and Encephalopathy [APE2] score”) prediz, com base na avaliação clínica e de neuroimagem, a necessidade de uma investigação específica com exame do líquido cefalorraquidiano e pesquisa de autoanticorpos:
Você também pode se interessar por: Sífilis: Diagnóstico das Complicações Neurológicas.
| Score APE | Pontos |
| Alterações rapidamente progressivas do estado mental nas últimas 1–6 semanas ou atividade convulsiva de início recente (no último ano). | 1 |
| Alterações neuropsiquiátricas: agitação, agressividade, labilidade emocional. | 1 |
| Disfunção autonômica (taquicardia atrial sustentada ou bradicardia, hipotensão ortostática, hiperidrose, pressão arterial persistentemente lábil, taquicardia ventricular, assistolia cardíaca ou dismotilidade gastrointestinal). | |
| Pródromo viral (rinorreia, odinofagia, febre baixa) na ausência de malignidade sistêmica subjacente nos últimos 5 anos. | 2 |
| Distonia braquiofacial. | 3 |
| Discinesias faciais na ausência de distonia braquiofacial. | 2 |
| Convulsões refratárias a pelo menos dois medicamentos anticonvulsivantes. | 2 |
| Achados no líquido cefalorraquidiano consistentes com inflamação (proteína > 50 mg/dL e/ou pleocitose linfocítica > 5 células/uL). | 2 |
| Câncer sistêmico diagnosticado dentro de 5 anos do início dos sintomas neurológicos (exceto carcinoma cutâneo de células escamosas ou basais e tumor primário ou metastático cerebral). | 2 |
| Escore máximo | 15 |
De acordo com o escore APE a conduta sugerida é:
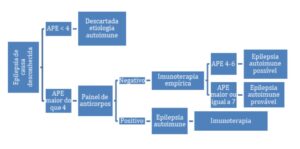
Os anticorpos específicos potencialmente associados com Epilepsia Autoimune são:
- anti-AMPA-R;
- anti-ANNA-1;
- anti-ANNA-2;
- anti-ANNA-3;
- anti-DPPX;
- anti-CASPR-2;
- anti-CRMP-5;
- anti-GAD65;
- anti-GABABR;
- anti-GABAAR;
- anti-GFAPα;
- anti-IgLON5;
- anti-LGI1;
- Anti-Ma-1 / Ma-2;
- Anti-MOG;
- anti-mGluR5;
- anti-NMDA-R;
- anti-PCA2.
Esses anticorpos devem ser testados no líquido cefalorraquidiano e no soro.
Confira a lista completa dos exames realizados pelo Senne Liquor.
Referências bibliográficas:
Geis C, Planagumà J, Carreño M, Graus F, Dalmau J. Autoimmune seizures and epilepsy. J Clin Invest. 2019;129(3):926-940.
Husari KS, Dubey D. Autoimmune Epilepsy. Neurotherapeutics. 2019;16(3):685-702.
Vezzani A, Fujinami RS, White HS, et al. Infections, inflammation and epilepsy. Acta Neuropathol. 2016;131(2):211-234.
Pack AM. Epilepsy Overview and Revised Classification of Seizures and Epilepsies. Continuum (Minneap Minn). 2019;25(2):306-321.


